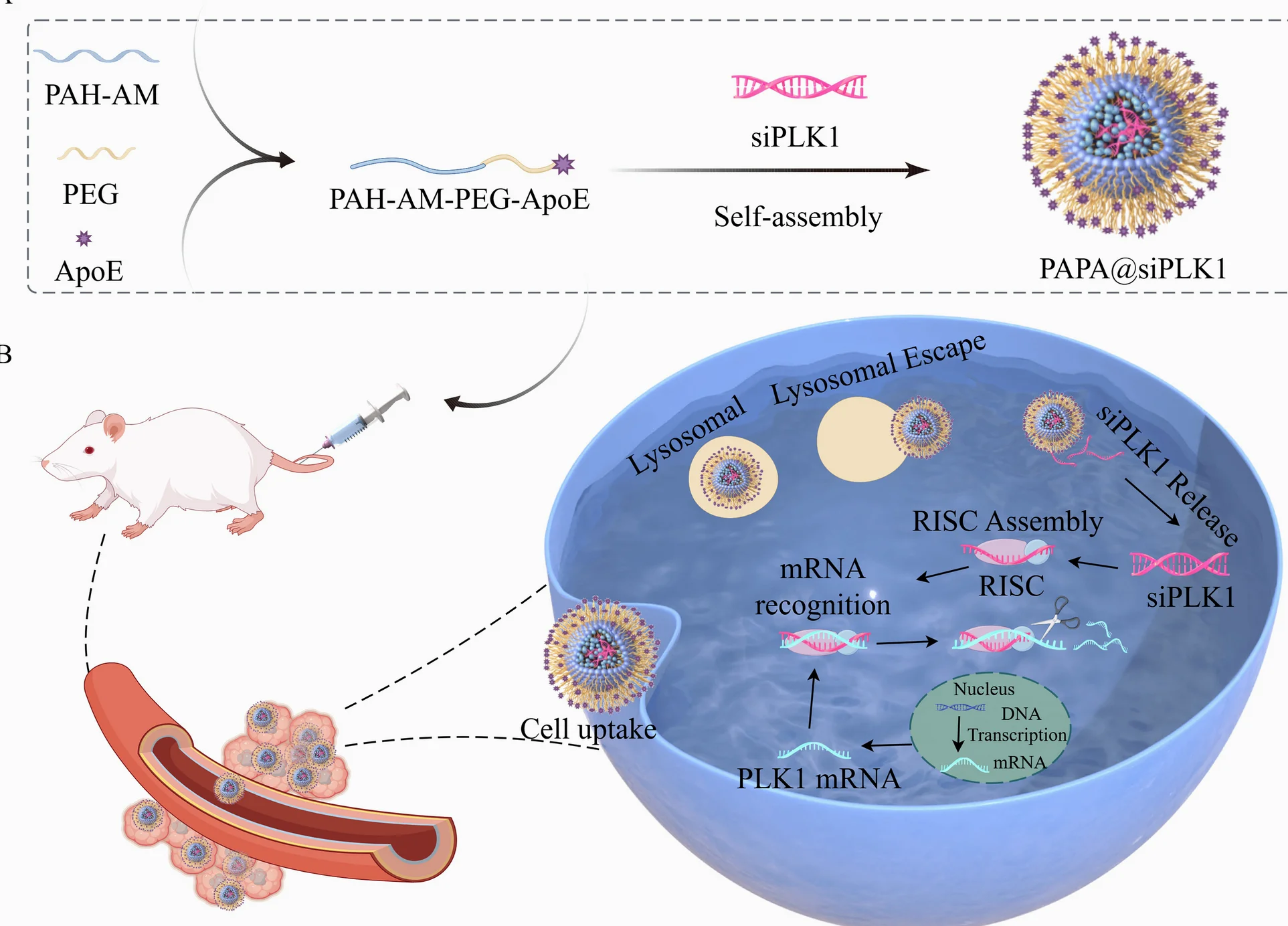
베이징 — 과학자들은 작은 간섭 RNA(siRNA)를 사용해 Polo-like Kinase 1 유전자를 억제함으로써 뇌종양 성장에 표적으로 작용하는 새로운 나노입자 전달 시스템을 개발했다. 연구팀은 PAH-AM-PEG-ApoE라는 캐리어, 즉 PAPA를 합성해 뇌종양 세포에 siPLK1을 직접 전달하는 방식을 사용했다.
이 캐리어는 연구팀의 실험실에서 특허를 받은 양이온성 폴리머인 PAH-AM을 기반으로 한다. 이에 폴리에틸렌 글리콜을 DMTMM을 응축제로 사용해 메탄올 기반 반응을 통해 결합시켰다. 트리에틸아민을 첨가한 후 온도를 3~5°C로 유지하며 22시간 동안 반응을 진행했다. 그 결과, 원심분리와 아세토니트릴 세척을 통해 정제된 PAH-AM-PEG이라는 노란 고체가 얻어졌다.
다음 단계로 ApoE(159-167) 펩타이드를 결합했다. 이 펩타이드는 Motif Biotech에서 제공받았다. 연구자들은 PAH-AM-PEG 3그램을 메탄올에 용해한 후 PBS-메탄올 용액에 있는 펩타이드와 혼합했다. 실온에서 43시간 동안 반응을 진행한 후 48시간의 다이알리시스를 거쳐 동결건조를 통해 풍부한 PAPA 분말을 얻었다.
siPLK1을 로드하기 위해 팀은 정전기 자가 조립 방식을 사용했다. 10mg의 PAPA를 DEPC 처리된 물에 용해한 후 무균 여과한 후 0.04mg의 siRNA와 1:1에서 3:1의 비율로 인큐베이션을 진행했다. 최적의 결합은 높은 비율에서 확인되었으며, 1% 겔을 100V로 30분간 전기영동한 후 UV 아래에서 겔이 발광하며 2.5:1 이상의 질량 비율에서 siRNA가 완전히 포획되었음을 확인했다.
Malvern Zetasizer Nano ZS를 이용한 입자 특성 분석은 전달에 적합한 크기와 제타 전위를 보여주었다. 스캐닝 전자 현미경은 나노구조의 형태를 캡처했다. 방출 테스트에서는 FAM 표지된 siPLK1이 pH 7.4의 PBS에서 다이알리시스 가방에서 천천히 누출되었다. 488/518nm에서의 형광 측정은 24시간 동안 누적 방출을 추적했다.
안정성은 두드러졌다. PAPA는 37°C에서 10μg/mL의 RNase A에 대해 siPLK1을 보호했다. 자유로운 siRNA는 겔 분석에 따르면 수시간 내에 분해되었지만, 나노입자는 6시간까지 화물을 보호했다. 혈청 안정성 분석은 더욱 견고함을 입증했다.
이 시스템은 Wuhan Pnosay에서 제공한 태아 소 혈청이 포함된 RPMI-1640에서 배양된 U87MG 인간 뇌종양 세포를 표적으로 한다. Yangzhou University에서 제공한 6~8주령의 BALB/C 마우스는 in vivo 테스트를 모델로 한다. 사용된 장비에는 도쿄의 Olympus 현미경과 뉴욕의 Thermo Fisher PCR 장비가 포함된다. siRNA 서열: siPLK1 sense 5′-CCCGAGGUGCUGAGCAAGAAAdTdT-3′, antisense 5′-UUUCUUGCUCUCAGCACCUCGGGGdTdT-3′. 음성 대조군 siNC는 무작위 서열을 사용했다.
뇌종양은 혈뇌장벽의 장벽으로 인해 여전히 치명적이다. PAPA에서의 ApoE 모방은 뇌 침투를 증가시킨다. PLK1 억제는 암 세포의 유전자 분열을 방해한다. 초기 데이터는 PAPA@siPLK1이 종양을 효과적으로 줄인다는 것을 시사한다. 전체적인 in vivo 결과는 출판을 기다리고 있다.
AAPS PharmSciTech에 발표된 연구에 따르면 이 플랫폼은 표적 치료를 발전시킨다. 연구자들은 합성 수율부터 겔 이동까지 모든 단계를 최적화했다. 형광 Cy7과 FAM 표지물은 세포와 마우스 내 전달을 추적했다.








댓글
아직 댓글이 없습니다
첫 번째로 의견을 남겨보세요